Neoris ayuda a las empresas a volver a las oficinas con su plataforma HEALTHCHECK
mayo 26, 2020
Sony presenta cámara para vloggers ZV-1, diseñada para creadores de contenido en video
mayo 26, 2020La FDA autoriza el uso de los ultrasonidos de Philips en pacientes con complicaciones pulmonares y cardiacas relacionadas con COVID-19

25 de mayo de 2020
- El portafolio de ultrasonidos de Philips, incluyendo la marca de tecnología portátil Lumify, ofrece valiosas herramientas de diagnóstico para profesionales sanitarios en primera línea de la pandemia.
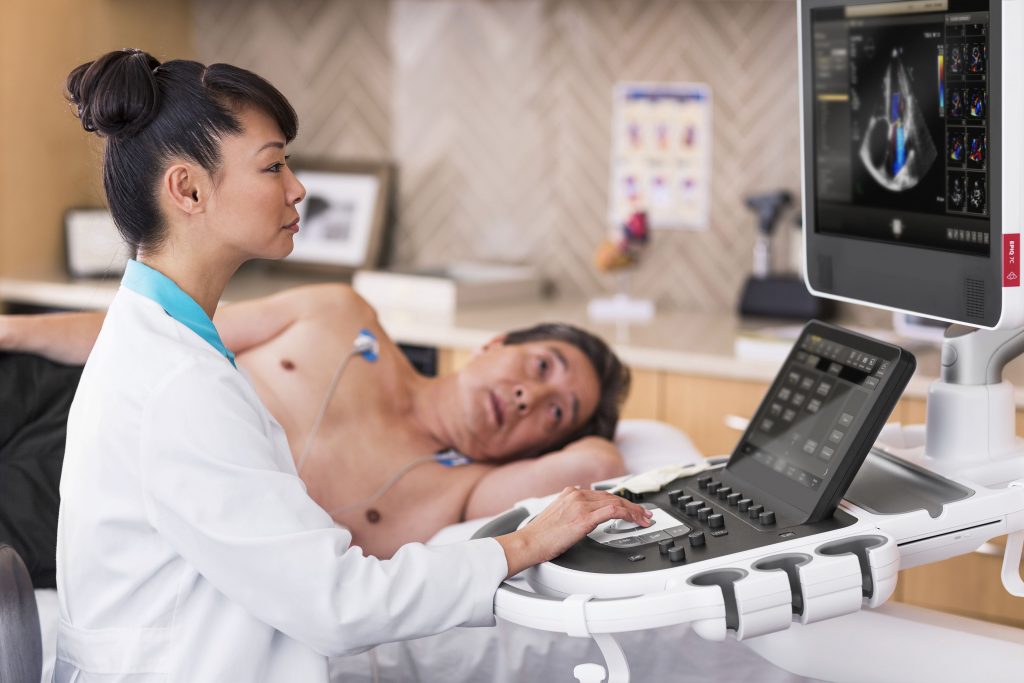
Ámsterdam, Países Bajos – Royal Philips (NYSE: PHG, AEX: A PHIA), líder mundial en tecnologías de salud, ha recibido autorización de las autoridades sanitarias de Estados Unidos (FDA, por sus siglas en inglés) para comercializar una amplia gama de equipos de ultrasonido para el tratamiento de complicaciones pulmonares y cardiacas relacionadas con la epidemia de COVID-19. Los equipos de ultrasonidos portátiles, en particular, se han convertido en una herramienta muy valiosa para los clínicos que tratan a pacientes con COVID-19 por su capacidad de visualización y fácil desinfección.
Como resultado de esta autorización por parte de la FDA, la primera concedida a un fabricante de equipos médicos, Philips puede proporcionar una guía práctica detallada para ayudar a los profesionales sanitarios que usan sus equipos y software en pacientes afectados por COVID-19. La autorización de la FDA se aplica a una gran gama de ultrasonidos de Philips, incluyendo las series EPIQ, Affiniti, Lumify, CX50 y Sparq, así como la solución del software de cuantificación avanzada QLAB.
Los ultrasonidos han demostrado su importancia en el diagnóstico por imagen de tejido pulmonar periférico afectado por neumonía, una manifestación clínica estrechamente relacionada con las complicaciones por COVID-19. Dado que el esfuerzo pulmonar puede derivar en disfunción cardiaca, los pacientes con COVID-19 tienen un mayor riesgo de padecer también complicaciones cardiovasculares. Un examen cardiológico por ultrasonidos puede ayudar a evaluar los efectos de la progresión de la enfermedad sobre la función cardiaca. Al realizar pruebas de ecografía a los pacientes con COVID-19 directamente en el lugar donde están siendo atendidos, por ejemplo, un box de emergencias o en la UCI, los clínicos pueden diagnosticarlos y monitorizarlos sin necesidad de moverlos de lugar, lo que contribuye a reducir el riesgo de transmisión del virus a otros pacientes o a los mismos profesionales sanitarios.
“Muchos centros sanitarios nos han comentado que nuestros ecógrafos de mano y portátiles están jugando un papel fundamental en sus esfuerzos contra el COVID-19”, afirma Bich Le, vicepresidente sénior y gerente general de ultrasonido en Philips. “Con esta autorización podemos ofrecer una guía clara y concisa para garantizar un uso seguro y eficaz de los ultrasonidos en diagnóstico y tratamiento de complicaciones pulmonares y cardiacas asociadas a COVID-19. Al mismo tiempo, estamos invirtiendo muchos recursos para ampliar su producción en todo el mundo, incluyendo en nuestras fábricas de Estados Unidos”, añade Le.
Con su amplia cartera, su liderazgo en áreas como los ecocardiógrafos y las capacidades exclusivas de la solución de ultrasonido de mano Lumify, Philips está perfectamente posicionada para apoyar a los profesionales sanitarios con soluciones tecnológicas necesarias para combatir la pandemia.
La solución de ecografía Lumify, que opera en conjunción con un smartphone o una tableta compatible, es el primer dispositivo de ecografía ultraportátil del mundo con funciones avanzadas de telemedicina. La plataforma de comunicación Reacts posibilita videollamadas bidireccionales con transmisión en directo de la ecografía, de forma que varios clínicos pueden ver a la vez la imagen por ultrasonido y la ubicación de la exploración, al mismo tiempo que discuten el resultado e interactúan. En el contexto de la pandemia por COVID-19, esta solución ayuda a minimizar el riesgo de transmisión del virus para el equipo médico.
La nueva guía desarrollada por Philips destaca los valores preestablecidos específicos, transductores, herramientas de cuantificación y otras posibilidades disponibles en los sistemas de ecografía de la compañía que son relevantes a la hora de evaluar y tratar complicaciones derivadas del COVID-19. Por ejemplo, el sistema premium de ecografía cardiaca EPIQ CVx incluye aplicaciones automatizadas para evaluación 2D del corazón, así como la posibilidad de realizar mediciones sólidas en 3D del volumen del ventrículo derecho y de la fracción de eyección.
La autorización concedida por la FDA abarca a los siguientes sistemas de ecografía de Philips: serie EPIQ, serie Affiniti, Lumify, CX50 y Sparq, así como soluciones específicas como el software de cuantificación avanzada QLAB. Para más información sobre cómo está respondiendo Philips a la pandemia de COVID-19, consulte el centro de información global de la compañía.
Para mayor información contactar a:
Noemí Vargas Muñoz Enrique Márquez Nicoli
noemi.vargas@fleishman.com enrique.marquez@fleishman.com
5540-6031 ext. 4904 ext. 4902
Acerca de Royal Philips
Royal Philips (NYSE: PHG, AEX: PHIA) es una empresa líder en tecnología de la salud, enfocada en mejorar la salud de las personas y en permitir mejores resultados a través del contínuum de la salud desde una vida saludable y prevención, hasta el diagnóstico, tratamiento y cuidado en el hogar. Philips aprovecha la tecnología avanzada y los profundos conocimientos clínicos y las perspectivas de los consumidores para ofrecer soluciones integrales. La empresa con sede en Holanda es líder en diagnóstico por imágenes, terapia guiada por imágenes, monitoreo de pacientes e informática de la salud, así como en salud del consumidor y cuidados en el hogar. Philips reportó ventas en 2019 por EUR 19.5 mil millones y emplea a aproximadamente 80,000 colaboradores con ventas y servicios en más de 100 países. Para más noticias de Philips visite www.philips.com/newscenter